相对于过去常用的肿瘤细胞接种和免疫缺陷小鼠模型,基因修饰小鼠(GEM)模型是建立在天然完整免疫条件下的原发(de novo)肿瘤,因此,作为肿瘤学研究的工具, GEM模型更能模拟人肿瘤的组织病理学和分子学特征,表现为有更好的遗传异质性,其优势在于能反映肿瘤细胞自身,以及肿瘤微环境中细胞等相互作用因素,包括具有引起原发肿瘤开始形成到发展为转移性疾病的能力。GEM模型的建立及应用极大促进了肿瘤学研究领域发展与进步。目前,GEM模型已成功应用于验证潜在肿瘤基因与药物靶点,考核治疗效果,分析肿瘤微环境影响,以及评价药物耐药性机制等研究领域。而且,结合临床病人研究与构建更加合理有效的GEM模型,优化肿瘤干预的临床前试验,无疑将进一步促进肿瘤治疗新策略的研发,提高其有效转化为临床上实际应用的成功率。
目前肿瘤学研究面临的主要挑战
肿瘤学研究及肿瘤治疗在临床上仍然面临着许多挑战,其中抗肿瘤药物耐受性的形成和肿瘤转移性疾病是当前面临的两个重要现实难题。抗肿瘤耐药性的产生是由于异质性肿瘤中的原发突变的出现,或治疗前耐药克隆的大量生长引起的,而现有的靶向抗肿瘤制剂的单一疗法,或化学药物疗法都无法避免药物耐受的发生。而且,在获得明显成功治疗之后,少量药物耐受肿瘤细胞可以存活下来,并在一定时间后,成为主要细胞群,形成与原始肿瘤表型不同的复发疾病。而肿瘤转移性疾病则是导致90%以上与癌症相关死亡的原因,因为现在对于这些继发肿瘤也多无有效的治疗方法。近年来,虽然针对干预肿瘤病人免疫系统的肿瘤免疫疗法取得了一些令人鼓舞的进展,但该疗法也只是在一些特定病例情况下有效果,而对于大多数肿瘤病人仍不具有实际临床意义。
所谓成功的肿瘤治疗往往需要多种方法的协同作用,比如手术,放射线照射,细胞毒性疗法,以及免疫疗法等综合策略。为了设计出有效合理的综合治疗措施与方案,首要的基础与前提是深入了解肿瘤的形成与发展,转移,及治疗应答过程中,肿瘤细胞自身及其微环境细胞间相互作用的机制,从而寻找针对不同肿瘤类型的有效的治疗方法。为了实现这一目的,研究者们就必须依赖于动物模型的临床前研究。尽管过去依赖于传统临床前小鼠模型(即通过建立移植人肿瘤细胞系或同种小鼠肿瘤细胞系模型等方法)获得了临床前抗癌新疗法的成功验证,但绝大多数的这些新疗法在临床III期试验中却都以失败而告终。
总体上讲,由于传统体内肿瘤小鼠模型在预测临床新疗法效果方面的表现不佳,因而更加凸显出寻找具有更好预测能力及效果的改进型临床前体内模型的意义与价值。在基因修饰技术方面的进步与发展,使得快速研制能更有效地模拟人肿瘤的GEM模型成为现实,GEM模型在遗传组成,肿瘤细胞与其肿瘤微环境的相互作用,药物反应及耐受等方面都更接近肿瘤病人。而新一代GEM模型的出现,也大大促进抗肿瘤新疗法策略转化为临床应用,达到提高癌症病人生存率的目的。
肿瘤学研究中常用传统小鼠模型的优势与不足
50年前首先在裸鼠体内移植人/鼠肿瘤细胞系而建立的小鼠肿瘤移植模型成为肿瘤研究中常用的小鼠模型,这类移植模型可快速测试潜在肿瘤及转移相关基因,并成为临床前的药物试验主要工具。例如,通过异种移植研究有助于揭示结肠癌(CRC)对药物(如Vemurafenib)在小鼠体内的耐受机制,从而实现在临床试验中对CRC病人启动同时针对突变BRAF(如V600E)和EGFR的靶向联合疗法,表明这类异种移植模型在建立新的联合治疗策略方面的实际意义。
异种移植研究也有助于发现特定基因表达特征,研究其介导的器官特异性定位转移的特点。如应用该种模型证实了传播的乳腺癌细胞存在于血管附近,这为调控这些传播的乳腺癌细胞提供了可能的对策。而且,应用肿瘤细胞系移植的体内模型研究,也为抗肿瘤免疫,T细胞耐受机制,肿瘤免疫逃逸途径等提供了许多基本的认识概念。这些发现都为目前进行中的肿瘤免疫疗法的突破奠定了基础。
然而,由于肿瘤细胞系一开始就含有许多突变,而且在体外长时间培养过程中,还会产生额外突变,因此,此类接种模型难以真实反映人肿瘤细胞的形态学和遗传异质性,从而降低了该类模型作为临床应用效果预测性的可靠性。另外,为了防止可能的排斥反应,肿瘤细胞系的异种移植模型是建立在免疫缺陷小鼠基础上,这也限制了其应用于肿瘤发展中免疫系统以及治疗应答等领域的研究。
不同于细胞系移植模型,通过将新鲜人肿瘤活检物移植至免疫缺陷小鼠构建的病人来源的肿瘤移植(Patient-derived tumor xenografts,PDTX,或PDX)模型则具有更多优势,PDX小鼠模型的肿瘤保留了来自肿瘤病人的肿瘤组织分子,遗传,组织学异质性等特征(甚至经过小鼠体内的传代几代之后)。所以,PDX模型也成为目前个性化医学和临床前药物筛选的有用工具。
目前,PDX模型的研究已大规模应用于潜在临床药物预测试验。有研究者通过构建约1000个来自不同类型突变的PDX模型,并应用这些不同的PDX模型对不同药物进行小鼠体内筛选,寻找药物与肿瘤基因型之间的关联性,以达到试验重复性和临床可解释性的统一。
不幸的是,PDX模型在研究某些类型肿瘤方面(如雌激素受体阳性的乳腺癌和前列腺癌)的不满意效果成为了限制其应用的主要障碍。而且,PDX模型必须建立在免疫缺陷小鼠上,这样的小鼠缺乏由获得性免疫系统介导的天然抗肿瘤与促肿瘤活动。
研究者们也明白,虽然PDX模型缺乏功能性的获得性免疫系统,该模型仍可为临床提供有价值的研究资料。正在进行中的相应改进是通过移植人CD34阳性造血干细胞或前体细胞的方法,重建人免疫系统的人源化的小鼠模型,并取得了显著的成功。虽然来自某些特异谱系的人免疫细胞在小鼠体内的重建仍具有挑战性,但通过引入人相关细胞因子,趋化因子,生长因子等方式,获得促进人骨髓细胞在小鼠体内发育与成熟的效果。
为了构建优化能够支持人HLA限制性T细胞发育的免疫缺陷小鼠,应用基因修饰技术建立人源化小鼠模型,将人HLA分子引入至敲除小鼠MHC类型I和II相应区域。人源化小鼠模型能作为免疫疗法临床前评价的有用工具,然而,当人造血干细胞供体来源(如通过脐带血或胎肝)有限时,其现实操作中的较高构建成本也自然成为该模型实际应用的不利因素了。
应用不断完善GEM模型研究原发肿瘤
上世纪70年代成功建立小鼠原核注射转基因技术以后,1980年代早期借助该方法第一次将克隆癌基因导入小鼠基因组中,成功制备了所谓的致癌小鼠(Oncomice)。 该致癌小鼠是应用乳腺特异性启动子(MMTV)特异性表达癌基因v-HRas的第一个肿瘤GEM模型,该致癌小鼠首次构建成功,并证实了该小鼠形成原发乳腺肿瘤,极大地振奋了肿瘤研究领域团体,因为此研究结果是第一次真正证明了癌基因在正常细胞中表达能产生肿瘤的假说。1992年伴随着小鼠胚胎干细胞(ES)基因打靶技术的突破发展,成功构建的肿瘤抑制基因(TSG)敲除小鼠,也证明了该类TSG基因在肿瘤发生过程中的重要作用。
虽然致癌小鼠和 TSG 敲除小鼠提供了非常有价值的理论依据,但这两种模型也存在其局限性。由于转基因技术获得的小鼠是使转入的外源基因表达在特定组织中所有的细胞中,TSG敲除小鼠则是灭活体内所有细胞中的相关基因。然而,现实肿瘤的形成过程是在个体中整个组织器官健康的前提下,由于某个单细胞中某种遗传变异的积累而导致的弥散肿瘤现象。为了符合肿瘤形成过程的实际情况,更有必要设计与构建更加合理或复杂的小鼠模型,比如能实现条件性的在体细胞灭活肿瘤抑制基因,或者激活(突变)致癌基因的所谓条件性GEM模型。条件性GEM模型构建的基本原理是将需要修饰基因两端分别加上loxP重组位点,在特定Cre重组酶存在的情况下,loxP两端之间的DNA就可被敲除,达到特定条件下灭活该基因的目的。应用这种模型的第一个成功的例子是应用Cre-loxP系统介导的体细胞灭活Apc基因而构建的小鼠结直肠癌模型。应用腺病毒载体实现Cre重组酶特异性表达于肠上皮细胞,组织特异性敲除APC基因,引起小鼠快速形成散在结直肠腺瘤,其特征与家族性结肠腺瘤性息肉病(FAP)病人有许多相似性。所以,通过发现特异性相关癌症基因的突变体,研究者们可构建在组织学、分子学以及临床上更能模拟肿瘤病人的相似特征的小鼠模型。
借助Cre-ERT融合蛋白诱导系统,研究者们可对体细胞中相关靶基因在特定时间与特定组织实施修饰,即将雌激素受体的突变激素结合区域与Cre重组酶融合在一起,建立可诱导调控的Cre重组酶表达系统,当在雌激素类似物(如Tamoxifen)存在的情况下,引起Cre重组酶活性在翻译后激活,发挥其识别loxP位点的作用,实现诱导性切割靶基因的目的。因此,LoxP小鼠(即靶基因DNA两端分别含loxP位点)的条件性基因修饰,通过在选择的时间里加入诱导剂Tamoxifen后,控制Cre-ERT的特异性表达,达到对靶基因进行时空与区域上的特定修饰的目的。
虽然Cre-loxP系统能用于多于一个基因的修饰,但因这种过程是同时发生的,所以难以完全模拟肿瘤多步骤形成过程中,突变是逐渐积累形成过程的特征。最近,研究者们利用可独立发挥作用的可诱导双重组酶系统(如Flp-FRT/Cre-loxP,或Cre-loxP/Dre-rox),建立了对靶基因表达实施先后调控的修饰方式。该技术方法成功应用的实际意义有如下几方面,1. 独立研究针对肿瘤细胞的自发和非自发通路及过程;2. 模拟人多步骤的癌症形成过程,有续地进行诱导突变;3. 开展独特的肿瘤治疗靶点遗传性评价。
肿瘤GEM模型构建策略与技术方面的改进
GEM模型因其独特优势已经被证实是肿瘤学研究的有效工具,但研究者们也一直努力对其进行着不断改进与完善。由于该类小鼠模型在构建与研制过程中周期长,工作量大,以及成本高等原因,特别是对于多个等位遗传位点进行修饰,构建具有遗传特性的新突变小鼠模型,研制过程更耗时,且需要更长久的交配繁殖过程。这也成为限制具有遗传能力的GEM模型广泛实际应用的一个主要因素。近年来,由于肿瘤基因组序列研究技术的广泛普及与应用,以及随着新发现的癌症相关基因突变数量的快速增长,更加需要建立快速新颖的小鼠模型研制策略,实现在体内快速验证潜在致癌基因,以及建立已知病人相关突变的非生殖遗传修饰GEM模型的目的。目前这方面的进展主要有:ES细胞为基础的肿瘤模型;应用CRISPR/Cas9技术基因组编程;肿瘤病人相关位点的改善肿瘤模型。
1. ES细胞为基础的肿瘤模型
为了进一步加快新型人肿瘤GEM模型的研制,将小鼠胚胎干细胞(ESC)经过基因修饰后而作为非遗传修饰(如嵌合体)小鼠直接进行肿瘤学研究已成为一种研究策略。最近报道的GEM-ESC策略,即建立以ES细胞为基础的肿瘤GEM模型。该类模型是在原有基因修饰的基础上,快速构建新型基因遗传修饰小鼠模型。例如,应用GEM-ESC策略,在原有K14cre-Brca1-Trp53(KBIP)的小鼠乳腺肿瘤模型的ESC上,直接导入MET原癌基因,构建新型KBIP-MET的转化乳腺癌模型。研究结果表明,与KBIP小鼠相比,此KBIP-MET小鼠形成的乳腺癌更具有转化特征,表现为更容易形成癌肉瘤。在对肿瘤药物的反应性上,KBIP小鼠模型的乳腺癌对临床RARP抑制剂(如Olaparib)敏感,而KBIP-MET小鼠模型的转化乳腺肿瘤则显示对该抑制剂具有耐受性。
2. 应用CRISPR/Cas9技术的基因组编程
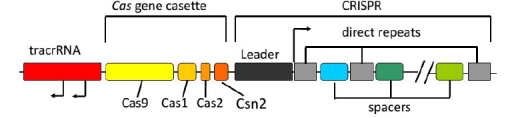
过去十年,伴随新的基因组编程技术(如ZFNs和TALENs)快速发展,2013年出现了CRISPR/Cas9基因组编程系统,该类基因组编辑技术成为继PCR技术发展以来,过去几年生物学研究领域的有革命性进步的及影响力较大的技术更新。CRISPR/Cas9系统首先发现于原核生物中针对抵抗外来入侵遗传物质而建立的免疫系统,并很快被成功用于各类物种的基因编辑。借助单一的引导RNA(sgRNAs), Cas9核酸酶能特异性作用于基因组任何基因位点,达到基因敲除的目的。通过应用Cas9诱导的DNA断裂和单链核苷酸/供体DNA,该系统也可实现对特定基因突变,或特定插入loxP/FRT重组位点等进行遗传修饰。
CRISPR/Cas9技术系统所表现出的同时对基因组不同位点进行有效编辑等基因打靶策略特征,使其立刻成为快速研制肿瘤小鼠模型的选择。目前在人肿瘤病人观察的所有遗传突变都可以通过基因修饰的方法来快速地构建相应的小鼠模型,包括条件性基因敲除,点突变,易位等。另外,也有研究者应用CRISPR/Cas9技术对小鼠的致癌基因和TSGs进行了体细胞(非生殖遗传性)编辑,因为此研究策略的努力与成功,使该系统成为研制肝细胞肿瘤,肺癌,脑癌,胰腺癌,以及乳腺癌的非遗传修饰模型的新方法。
最近,CRISPR/Cas9系统也应用于靶基因的抑制(CRISPRi)或激活(CRISPRa)的遗传修饰。这类修饰系统可用于研制相应致癌基因,和/或抑制TSGs基因的诱导和可逆激活小鼠模型。比如借助CRISPRa为基础的系统,通过激活致癌基因的转录,达到研究其致癌潜力的目的。
虽然CRISPR/Cas9为基础的基因编辑系统非常具有潜力,但该系统应用于体内基因编辑也存在一定的缺陷,比如,目前该系统策略不适合于验证潜在致癌基因的致癌潜力。另外,将Cas9导入体细胞的基因编辑方式,可引起Cas9特异性免疫反应,导致Cas9表达细胞有被清除的可能性。为了避免这些可能的潜在风险,可选择在免疫缺陷小鼠体内进行相应的实验,或通过基因修饰方法,首先获得对Cas9具有免疫学耐受小鼠模型后,再开展相应的动物实验。最后,虽然已有报道表明,应用引起DNA单链断开的可诱导Cas9n缺口酶,可以降低其脱靶效应, 但研究者在实际应用中必须有清晰认识,要想完全避免由CRISPR/Cas9介导的非设计所需要的脱靶突变是很难的。
3. 肿瘤病人相关位点的改善肿瘤模型
构建理想的肿瘤病人相关突变模型,对研究靶基因在肿瘤发生过程中的作用,以及有效评价药物效应就显得很有必要性与实际意义。因为在人肿瘤抑制基因(TSGs)中,许多具有肿瘤形成依赖的生殖细胞突变和体细胞突变都是错义或无义突变,从而导致突变产物或可能带有功能截短蛋白的形成。这类突变现象是难以通过条件性敲除小鼠模型来实现的,因为条件性基因修饰策略是将靶基因中某个或几个外显子完全敲除,达到灭活靶基因功能。一些研究结果已经表明,参照肿瘤病人相关TSG突变构建的小鼠突变模型,可产生与靶基因完全敲除不同的表型。比如,与Trp53基因敲除小鼠比较,病人相关的Trp53热点突变小鼠表现有更加明显的致癌活性。
同样,构建BRCA1乳腺癌病人相关的Brca1基因突变的条件性小鼠模型研究表明,与Brac1完全敲除小鼠模型相比,因Brac1基因中特定RING区域引入突变而引起的乳腺肿瘤,更容易对那些破坏DNA的药物产生耐受性,因为其BRCA1蛋白含有较少的RING活性的缘故。研究也证实,由于突变导致Brac1蛋白含有较少的RING活性 ,表现为更容易对那些破坏DNA的药物产生耐受性,该结果有助于揭示这些突变与治疗反应效果之间的因果关系。